Infektionsprophylaxe bei tracheotomierten Patienten in der häuslichen Versorgung
von Ulrich Meng
Die Anlage eines Tracheostomas ist ein massiver Eingriff in das Leben des Patienten und das seines direkten Umfeldes, wie beispielsweise Familie und Freunde. Die gesamte Lebenssituation ändert sich drastisch, da sich durch den operativen Eingriff viele körperliche Veränderungen einstellen. Diese Situation führt oft zur sozialen Isolation, da es schwer ist, mit einem „Loch im Hals“ zu leben und umzugehen. Im Laufe der letzten Jahre haben einige medizintechnische Firmen innovative Produkte entwickelt, die Tracheotomierten das Leben angenehmer oder auch wieder lebenswert machen.
Eine besondere Rolle spielen dabei Maßnahmen zur Verhütung von Infektionen, denn diese können sowohl den gefährdeten Patienten als auch das Anlegepersonal mehr als notwendig belasten. Im Folgenden werden einige Maßnahmen und Produkte zur Verringerung der Infektionsgefahr erläutert, ohne dass dabei ein Anspruch auf Vollständigkeit erhoben wird.
Patienten, die künstlich beatmet werden, benötigen geblockte Trachealkanülen mit einem so genannten Cuff (engl. Manschette) an deren Ende. Bei beatmeten Patienten wird durch den Cuff ein seitliches Entweichen der Atemgase verhindert. Grundsätzlich muss hier dafür gesorgt werden, dass der Beatmungsdruck nicht an der Kanüle vorbei nach oben entweichen kann. Auf diese Weise kann sichergestellt werden, dass die Atemluft die Lungen erreicht und der Patient mit ausreichend Sauerstoff versorgt wird. Das wird auch bei einer erhöhten Hustenreflexschwelle, beispielsweise bei einer Sedierung, genutzt. Aber auch nichtbeatmete (also spontanatmende) Patienten benötigen oft eine geblockte Trachealkanule, da die weiterhin bestehende Verbindung des Nasen-Rachen-Raumes zum Luftweg beispielsweise nach teilweiser Entfernung des Kehlkopfes, bei Kehlkopfanomalien oder (neuronalen) Schluckstörungen den Nachteil der Aspirationsgefahr mit sich bringt: Hier hat der Cuff die Aufgabe, die Luftröhre in Richtung Lunge abzudichten, um zu verhindern, dass bei Patienten mit Schluckstörungen Speisereste oder Speichel in die Lunge geraten.
Komplikationen bei tracheotomierten Patienten
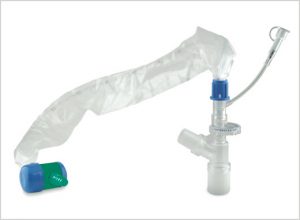
Die nicht mehr den natürlichen Gegebenheiten entsprechenden Atemwege und auch der „Fremdkörper“ Tracheostomiekanüle selbst können sowohl beim Tracheostoma als auch in den unteren Luftwegen Komplikationen verursachen, die aber durch fachgerechte Pflege und den Einsatz geeigneter Produkte minimiert werden können.
Stomainfektionen können bei der Anlage oder Pflege des Tracheostomas sowie durch die Abwehrschwäche des Patienten und Hospitalismuskeime gefördert werden. Die Infektionen können von Wundinfektion am Tracheostoma, örtliches Absterben von Gewebe bis hin zur blutigen oder eitrigen Tracheobronchitis und Pneumonie (Lungenentzündung) reichen.
Trachealstenose (Verengungen der Luftröhre) und Druckulcera (Druckgeschwüre) gelten als typische Spätkomplikationen, die hauptsächlich im Bereich des Tracheostomas oder des Cuffs auftreten. Die Ursache sind oft Druckschäden durch die Blockermanschette. Dabei wird z. B. die Luftröhre durch einen zu stark aufgeblasenen Cuff aufgedehnt, woraus u. a. Geschwüre entstehen können. Diese können auch durch asymmetrisches Aufblasen des Cuffs (nach Überblähung und daraus folgender Beschädigung), zu starken Cuffdruck oder ein Verrutschen der Trachealkanüle verursacht werden.
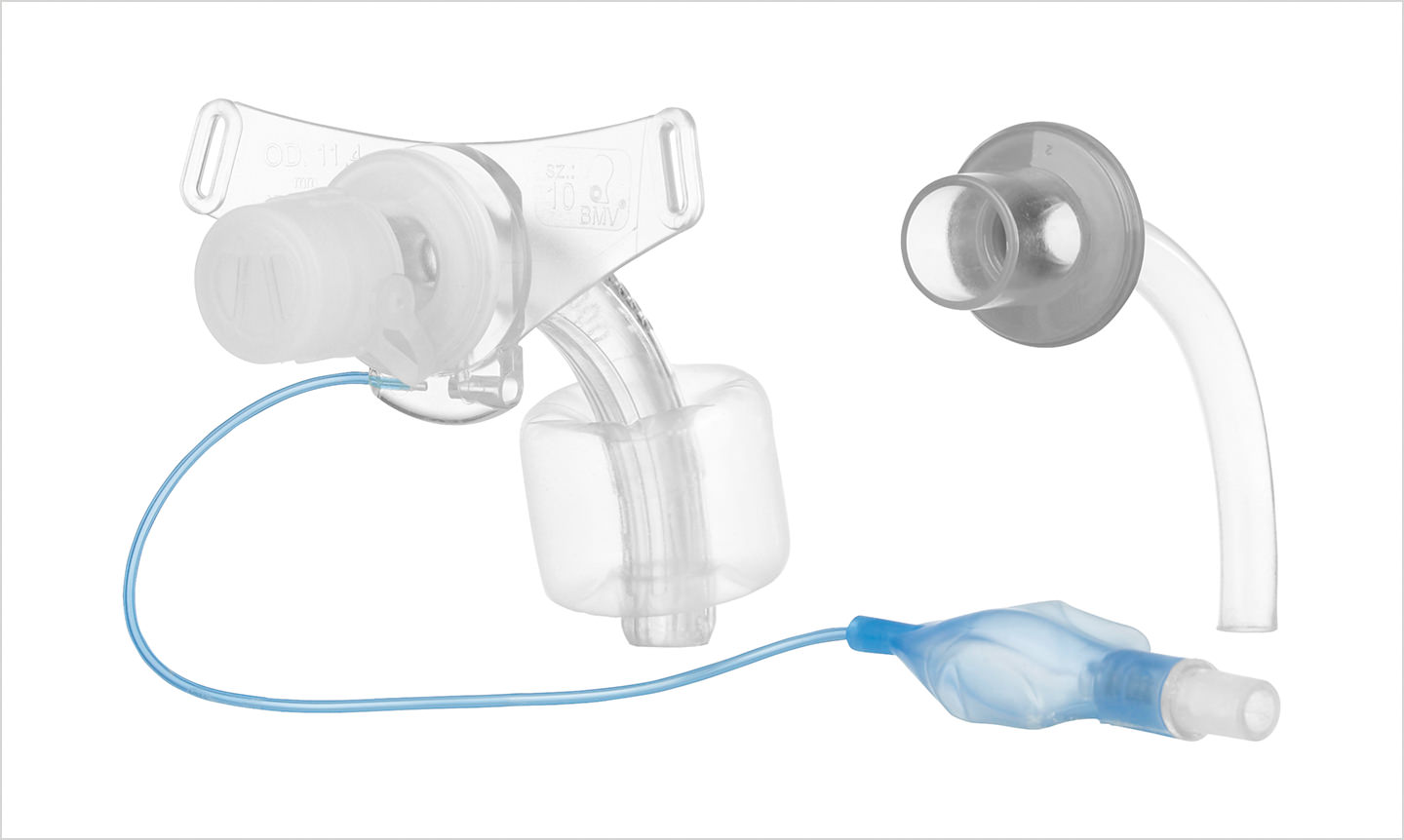

Abb. 2 Tracheostomiekanülen mit Innenkanüle
Pneumonien entstehen auf verschiedenen Wegen. Einerseits unter anderem durch eine ungenügende Abdichtung des Cuffs gegen durchsickerndes Trachealsekret aus dem Raum unterhalb des Kehlkopfes (subglottischer Raum), aber auch durch Austrocknung der Schleimhaut der Luftröhre und der unteren Atemwege, da ja die natürliche Funktion der Nase (Anfeuchtung, Reinigung, Erwärmung) durch die Trachealkanüle umgangen wird.
Auch wenn man davon ausgehen kann, dass insbesondere der Patient in der häuslichen Pflege in einem ihm vertrauten Keimspektrum lebt, kann doch bei geschwächtem Immunstatus oder einer entwickelten Resistenz (Unempfindlichkeit) dieser Erreger gegen Medikamente, eine Infektion begünstigt werden. Alle Komplikationen sind mit einem erhöhten Pflegeaufwand und damit auch höherer Kostenbelastung der Krankenkassen verbunden. Das gilt besonders bei einer dadurch notwendigen stationären Einweisung ins Krankenhaus, z. B. wegen einer Lungenentzündung. Die dort notwendige Behandlung kann leicht 10.000 bis 15.000 Euro kosten, die notwendigen Medikamente (Antibiotika) kosten ca. 400 Euro täglich [1].
Maßnahmen zur Verringerung der Infektionsrate bei tracheotomierten Patienten
Absaugung/Bronchialtoilette
In Lunge und Luftröhre wird natürlicherweise Schleim und Sekret produziert, der die eingeatmete Luft reinigt, indem er Partikel einfängt und nach oben transportiert, wo dieser Schleim abgehustet oder verschluckt wird. Diese Schleimproduktion ist bei fehlender Nasenfunktion (wegen der Trachealkanüle) meist erhöht. Um trotzdem die Atemwege frei zu halten und Infektionen sowie nicht beatmete Lungenbereiche zu vermeiden, muss das Sekret bei Patienten, die nicht abhusten können, abgesaugt werden. Das geschieht einige Male am Tag bis mehrmals stündlich. Manche Patienten empfinden das Absaugen als schmerzhaft und sehr unangenehm. Daher sollte nur abgesaugt werden, wenn Sekret wirklich vorhanden ist. Die Maßnahme muss natürlich steril und so schonend als möglich für den Patienten durchgeführt werden. Dabei ist eine Absaugung sowohl mit geschlossenem als auch mit offenem System möglich. Allerdings unterscheiden sich beide Verfahren in Kosten und Infektionsrisiko, auch für den Durchführenden.
Bei geschlossener Absaugung ist eine Keimübertragung zum Pflegenden vermeidbar, da das beim Absaugvorgang unvermeidlich entstehende keimbelastete Aerosol (Sprühnebel) im System verbleibt und nicht in die Umgebung gelangen und eingeatmet werden kann. Das Tragen einer Schutzbrille durch die Pflegekraft ist damit ebenfalls überflüssig. Der Absaugvorgang ist durch die besondere Art des Absaugkatheters sehr schleimhautschonend. Eine anschließende Spülung mit Sterilwasser bzw. Kochsalzlösung ist ebenfalls ohne eine Öffnung des Systems einfach durchzuführen, wodurch ebenfalls das Infektionsrisiko für den Patienten verringert werden kann. Demgegenüber ist die Absaugung mit offenem Absaugschlauch (Katheter) preiswerter, allerdings nur auf den ersten Blick. Denn während beim geschlossenen System eine Verwendung über den ganzen Tag (zum Teil auch länger) möglich ist, ist beim offenen System jedes Mal ein neuer Absaugschlauch (Katheter) notwendig, weiterhin entsprechende Schutzmaßnahmen (Handschuhe, Schutzbrille) beim Pflegepersonal. Außerdem ist auf ein atraumatisches (schleimhautschonendes) Absaugen zu achten, was besondere (und damit wieder teurere) Katheter voraussetzt.
Das Tracheostoma selbst ist nicht grundsätzlich als eine entzündete Wunde anzusehen. Das gilt sowohl für mittelfristig bestehende Tracheotomieöffnungen (nach Punktionstracheotomie) als auch für chirurgisch angelegte vernähte Tracheotomien bei Patienten, die diese Öffnung dauerhaft erhalten haben. Wenn ein Tracheostoma infiziert ist, sollten die Regeln der modernen Wundversorgung angewandt werden. Ein Großteil der Tracheostomainfektionen wird durch Manipulationen an der Stomaöffnung hervorgerufen. Auch das Wechseln der Kanüle zur Reinigung ist eine der Ursachen für diese Komplikation. Deshalb bringt die Verwendung von Trachealkanülen mit Innenkanüle hier entscheidende Vorteile bei der Handhabung durch seltenere Manipulation an der Kanüle. Dabei kann der innen liegende Teil (Innenkanüle) entnommen werden, ohne dass die eigentliche Trachealkanüle entfernt werden muss. Ein weiterer Vorteil ist der schnelle Zugriff bei Verstopfung oder Verlegung der Kanüle. Außerdem lasst sich bei gefensterten Varianten (Sprechkanüle) die gefensterte Innenkanüle leicht gegen eine ungefensterte austauschen, z. B. vor den Mahlzeiten. Dies ist auch ein entscheidender Vorteil im Überleitmanagement in den Normalstationsbereich oder die häusliche Versorgung.
Anfeuchtung

Durch die Trachealkanüle werden die oberen Luftwege überbrückt bzw. umgangen. Ihre Funktionen müssen durch künstliche Maßnahmen ersetzt werden. Eine Anfeuchtung, Erwärmung und Reinigung der eingeatmeten Luft ist entweder passiv (künstliche Nase/HME) oder auch aktiv (Atemluftbefeuchter oder Ultraschallvernebler) möglich. Eine Kombination beider Verfahren ist nicht sinnvoll. Künstliche Nasen (HME = Heat- and -Moisture-Exchanger) bieten einen guten Wärme- und Flüssigkeitsaustausch. Die Wärme und Feuchtigkeit der Ausatemluft wird zurückgehalten und wieder an die eingeatmete Luft abgegeben. Die hohe Feuchtigkeitsrückgewinnung reduziert das Risiko der Krustenbildung an Trachealkanüle oder Luftröhre, wodurch auch die Absaugvorgänge erleichtert werden. Vor allem beim nichtbeatmeten Patienten ist ein möglichst geringvolumiger HME anzustreben, um das Totraumvolumen (an dem Atemluftwechsel nicht beteiligter Luftanteil) klein zu halten.
Aktive Luftbefeuchter
Bei starker und/oder zäher Sekretion, erschwerter Einatmung oder beim Atemtraining müssen die Patienten mehrmals am Tag die Atemluft zusätzlich aktiv mit Ultraschallverneblern, Inhalatoren oder medizinischen Raumluftbefeuchtern anfeuchten. Um Infektionen weitgehend auszuschließen, muss bei Ultraschallbefeuchtern steriles Wasser verwendet werden. Als Faustregel gilt: Optimale Raumluftfeuchtigkeit liegt bei ca. 60 Prozent, die minimale Raumluftfeuchtigkeit bei ca. 50 Prozent. Als Beurteilungskriterium ist hier entscheidend, wie zäh das Sekret ist. Durch die Trachealkanüle verliert der Patient bis zu 75 Prozent der physiologischen Befeuchtungsleistung der oberen Atemwege. Diese fehlende Feuchtigkeit kann zu Austrocknungen, Schädigung der Atemwege oder Kanülenverschluss führen. Daher ist eine Anfeuchtung des Trachealsekretes durch eine Aerosoltherapie unbedingt erforderlich [4]. Dies dient der Erhaltung des natürlichen Reinigungsvorganges in den unteren Atemwegen und reduziert dadurch die Infektionsgefahr. Neue medizinische Ultraschallvernebler tragen mit einem Teilchenspektrum zwischen 1 – 6 pm tief in den Bronchiolen zur Sekretlösung bei. Deshalb ist ein geschlossenes Sterilwasser unbedingt erforderlich. Handelsübliche Luftbefeuchter, z.B. aus dem Baumarkt, bergen die Gefahr von zusätzlichen Infektionen, da bereits Falle von Lungenbläschenentzündungen (Alveolitis) auftraten.
Cuffdruck
Überwachung und Einstellen des Cuffdruckes
Der Cuff verhindert, dass Sekret oder Flüssigkeit in die Trachea eindringen kann oder während der Beatmung Luft aus der Trachea entweicht. Damit es nicht zur Schädigung der Trachea kommt, werden nur Trachealkanülen mit Niederdruckmanschetten verwendet. Der Cuffdruck kann mit einem speziellen Manometer gemessen werden und sollte bei ca. 20 mmHg liegen. Das sollte mehrmals am Tag geschehen. Eine Einstellung ,,nach Gefühl”, indem per Fingerdruck die Füllung am so genannten Kontrollballon geprüft wird, ist nicht möglich. Die resultierenden Cuffdrucke sind meist viel zu hoch [7]. Nur bei richtigem Cuffdruck ist eine ungestörte Durchblutung der Trachealschleimhaut gewährleistet.
Selbsttätige Systeme zur Cuffdruckregelung
Alternativ existieren selbstregelnde Systeme, die in einem weiten Bereich sowohl eine zu niedrige als auch eine zu hohe Blockung verhindern. Trachealkanülen mit entsprechendem System sind als ,,Lanz”-Kanülen auf dem Markt.
Dabei beschränkt sich die Cuffdruckkontrolle auf eine Sichtkontrolle des inneren Reservoirballons. Mit ,,Lanz-System“ wird jederzeit ein Cuffdruck zwischen 20 mmHg und 23 mmHg gewährleistet. Aber auch elektrische Geräte zur Druckregulierung sind möglich.
Neue Materialien
Relativ neu auf dem Markt sind Trachealkanülen mit einem Cuff, der nicht mehr wie bisher aus PVC, sondern aus Polyurethan besteht. Dieses Material bietet die Möglichkeit, auch mit deutlich geringeren Cuffdnicken als gemeinhin üblich, eine Blockung zu gewährleisten. Das funktioniert zum Teil bereits ab einem Cuffdruck von 10 mmHg, so dass eine weitgehende Schonung der Schleimhaut der Luftrohre möglich ist [2]. Auch dadurch ist eine Verringerung von Drucknekrosen oder Irritationen und damit von Infektionen möglich. Weiterhin bietet dieses Material auch in Bezug auf die Dichtheit Vorteile, worauf weiter unten eingegangen werden soll.
Absaugung des subglottischen Raumes
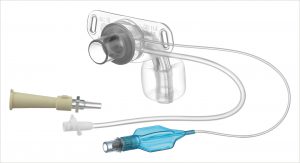
Eine nicht zu unterschätzende Rolle bei den Ursachen für eine Pneumonie spielt die Sekretansammlung im Raum unterhalb der Stimmlippen und oberhalb des Cuffs. Dieser Bereich wird subglottischer Raum genannt und ist mit Absaugkathetern nur schwer oder gar nicht zu erreichen, so dass dort immer ein Großteil des Sekretes das i. A. erhebliche Mengen Erreger enthält, verbleibt. Deshalb wird dieser Bereich auch ,,Jammerecke” genannt. Da auch ein optimal geblockter Cuff durch die kleinen Fältchen des Cuffmaterials im Laufe der Zeit Sekret in Richtung Lunge hindurch lässt, ist vor allem beim bettlägerigen Patienten eine Pneumonie (Lungenentzündung) nur eine Frage der Zeit. Dieser Vorgang wird als „stille“ Aspiration oder Mikroaspiration bezeichnet [6].
Was liegt also näher, als mit einem zusätzlichen Absaugkanal oberhalb des Cuffs der Kanüle dieses Sekret abzusaugen? Solche Kanülen werden als EVAC-Kanülen bezeichnet. In vielen Untersuchungen konnte gezeigt werden, dass die Anzahl der Patienten, die eine (nosokomiale = im Krankenhaus oder Pflegeheim erworbene) Pneumonie erleiden, mit einer entsprechend häufigen subglottischen Absaugung auf ca. 50 Prozent gesenkt werden kann. Deshalb hat dieses Verfahren längst Einzug in die amerikanischen Richtlinien zur Pneumonievorbeugung [3] gefunden. Auch in Deutschland ist das Verfahren inzwischen durch viele Untersuchungen untermauert [5].
Dichter Cuff
Eine zweite Möglichkeit, die Mikroaspiration deutlich zu verringern, besteht in der Verwendung von Kanülen mit dem bereits oben genannten neuen Cuffmaterial (Polyurethan). Bei diesem Material, das im Gegensatz zum PVC-Cuff nur noch ca. 10 pm dick ist (zum Vergleich: PVC 50 – 120pm) haben die Fältchen des Cuffs bereits bei dem beschriebenen niedrigen Cuffdruck ebenfalls eine Größe von nur etwa 10 pm. Dadurch wirken dort Kapillarkräfte, die ein Durchsickern von Flüssigkeit, und erst recht von dickerem Sekret, weitestgehend unterbinden. Das hat zur Folge, dass fast kein Sekret in die unteren Atemwege gelangt. In Verbindung mit einer subglottischen Absaugung ist dieses Sekret einfach abzusaugen, wodurch ein sehr guter Schutz vor Mikroaspiration erreicht werden kann. Unter diesen Voraussetzungen ist es notwendig, die Durchführung der subglottischen Spülung, z. B. mit antibiotischen Lösungen, neu zu diskutieren.
Die beschriebenen Maßnahmen werden nur in Verbindung mit anderen vorbeugenden Strategien, wie z. B. strikte Händehygiene, Lagerungsregime, Stressulkus-Prophylaxe, zum Erfolg führen und das Risiko zusätzlicher Erkrankungen, vor allem durch eine Pneumonie, senken. Die Auswahl der richtigen Kanüle, die Art der Atemgasklimatisierung und des atraumatischen Absaugens spielen eine entscheidende Rolle bei der qualitativen, aber auch ökonomisch sinnvollen Versorgung. Die vorbeugende Verhinderung von Komplikationen in der Intensivmedizin und die fachlich kompetente Überleitung in den häuslichen Bereich machen Netzwerke notwendig, die auch die Hausärzte einbeziehen. Dafür sind gemeinsame Fortbildungskonzepte zu entwickeln. Dabei kann die Broschüre ,,Leitlinie für die Versorgung von tracheotomierten und laryngektomierten Patienten” des Bundesverbandes Medizintechnologie e.V. (BVMed) Hilfe leisten.
Zusammenfassung
Die Versorgung tracheotomierter Patienten, ob im Bereich der Krankenhausbehandlung oder in der häuslichen Versorgung, ist letztlich eine Frage, wie konsequent die Umsetzung der Behandlungskette nach ärztlichen und pflegerischen Belangen gelingt. Eine Vielzahl von einfachen Maßnahmen ist bereits dazu geeignet, die Infektionsrate zu senken. Vor allem Maßnahmen zur Aufrechterhaltung der Funktion der Schleimhaut der Luftröhre und der Lunge und zur Verhinderung des Eintritts von Sekret in die unteren Atemwege mit allen daraus resultierenden Komplikationen sind im Hinblick auf die Gefahr für den Patienten, aber auch die Kosten der Pneumoniebehandlung unbedingt notwendig. Sie können nicht zuletzt einen wichtigen Beitrag zum Wohlbefinden des Patienten leisten.
Der Autor:
Ulrich Meng ist verantwortlicher Produktmanager für TRACHEOCUR<sup>®</sup>.
Sekundärliteratur
[1] Cocanour, C., L. Ostrosky-Zeichner, M. Peninger, et al.: Cost of a ventilator-associated pneumonia in a shock trauma intensive care unit, Surgical Infections 6 (2005), 65-72
[2] Dullenkopf, A., A. Schmitz, M. Frei, A. C. Gerber, M. Weiss: Air leakage around endotracheal tube cuffs, European Journal of Anaesthesiology, 21 (2004), 448-453
[3] Guidelines for Preventing Health- Care-Associated Pneumonia, 2003, Recommendations of CDC and the Healthcare Infection Control Practices Advisory, Committee, originated in the National Center for Infectious Diseases
[7] Häusliche Pflege Heute (2003), Urban & Fischer-Verlag, 549
[4] Mattner, F., P.Gastmeier: Empfehlungen zur Prävention nosokomialer Pneumonien, Anästhesiol Intensivmed Notfallmed Schmerzther 40 (2005), 79-84
[5] Smulders, K, H.van der Hoeven, I. Weers-Pothoff, C. Vandenbroucke- Grauls: A randomized clinical trial of intermittent subglottic secretion drainage in patients receiving mechanical Ventilation, Chest. 121 (2002), 858-862
[6] Stewart S. L., J. A. Secrest, B. R. Norwood, R. Zachary: A comparision of endotracheal tube cuff pressures using estimation techniques and direct intracuff measurement, AANA Journal, 6, Val. 71(2003), 443-447
